Ultra HiFidelity PCR -sett
Funksjoner
■ Enkel å betjene: Dette settet leveres som 2 × forblanding, og PCR kan utføres ved å legge til maler og primere.
■ High fidelity: Troverdigheten er 50 ganger den for Taq -polymerase.
■ Høy spesifisitet: Utmerket hot-start-ytelse for å sikre produktspesifisitet.
■ Rask forsterkning: Forlengelseshastigheten kan nå 10-15 sek/kb.
■ Sterk utvidbarhet: Opptil 20 kb DNA -fragmenter kan forsterkes.
■ Bred bruk: Settet inneholder PCR Enhancer og er egnet for forsterkning av høy GC og komplekse maler.
Spesifikasjon
Type: High fidelity DNA -polymerase
Forsterkningshastighet: 10-15 sek/kb
Fragmentstørrelse: <20kb
Søknader: High fidelity PCR-forsterkning, genkloning, høy GC-malforsterkning, genkloning av komplekse genomer, cDNA high fidelity-forsterkning, SNP-deteksjon, stedsspesifikk mutasjon, etc.
DNA -ekstraksjonsutbytte fra forskjellige plantevev:
Merk: DNA -utbyttet avhenger av prøvetyper. Alt materialet ovenfor er fra ømme blader.
Alle produktene kan tilpasses for ODM/OEM. For detaljer,vennligst klikk på Tilpasset service (ODM/OEM)
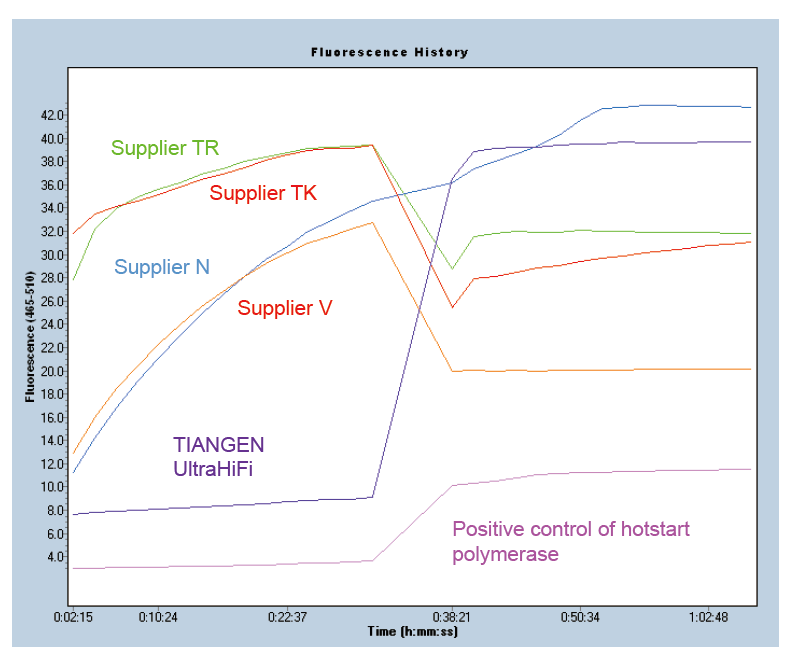 |
Hot-start for å sikre produktspesifisitet Figur 1. Ultra HiFi har utmerket varmstartfunksjon for å sikre spesifisiteten til forsterkningsprodukter. Molekylær beacons -metode ble anvendt (Ma et al., Anal Biochem, 2006). |
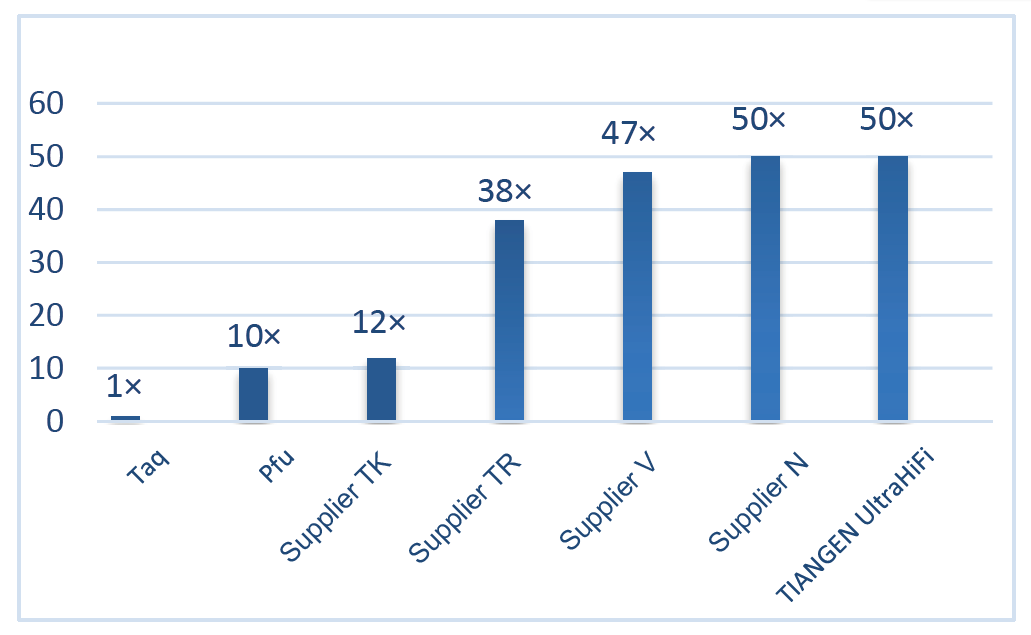 |
Utmerket high fidelity, 50 ganger høyere enn Taq Polymerase Figur 2. Troverdigheten til Ultra HiFi er 50 ganger høyere enn for vanlig Taq -polymerase. Polymerisasjonstroheten til Taq -polymerase (uten korrigerende aktivitet) brukes som referanse. |
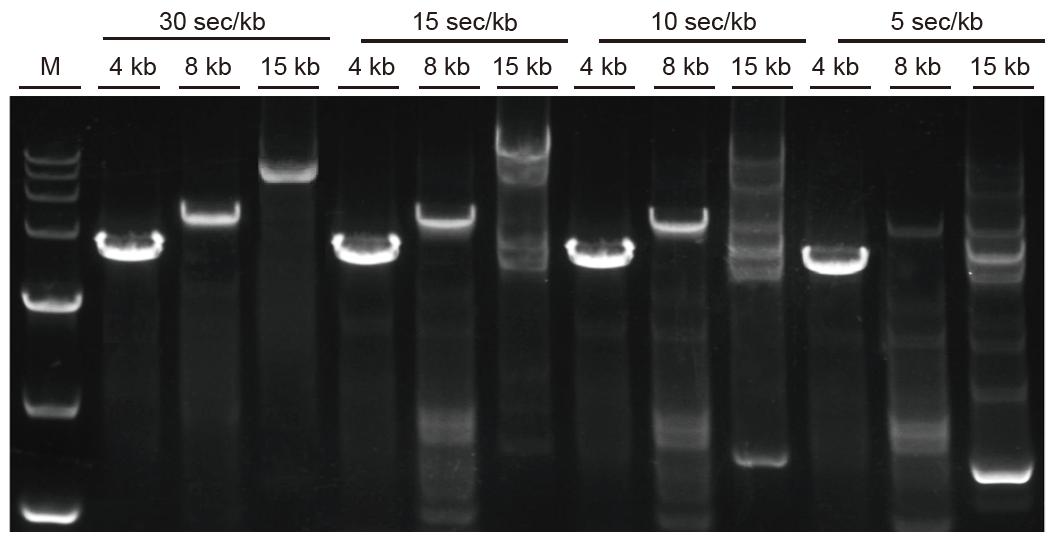 |
Rask forsterkning og lange fragmenter kan forsterkes raskt Fig. 3. Ultra HiFi kan strekke seg opptil 5 sek/kb for fragmenter mindre enn 4 kb. For lange fragmenter kan forsterkningstiden forlenges på passende måte. For fragmenter på mer enn 15 kb kan hastigheten være opptil 30 sek/kb. M: TIANGEN D15000 markør |
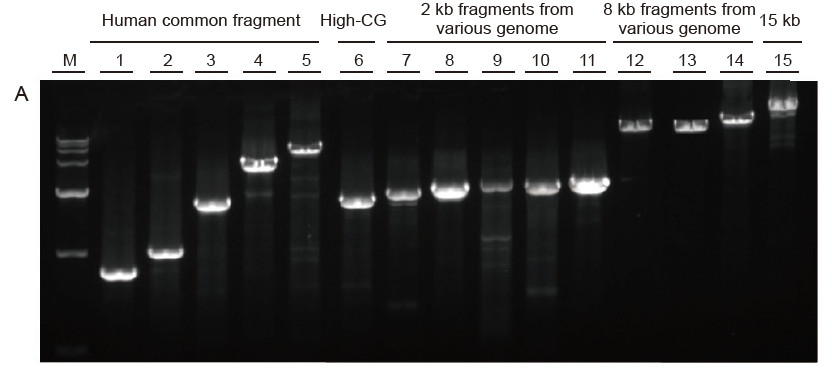 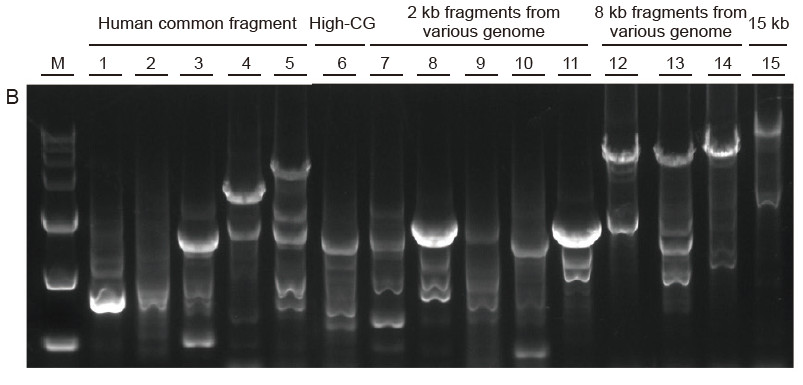 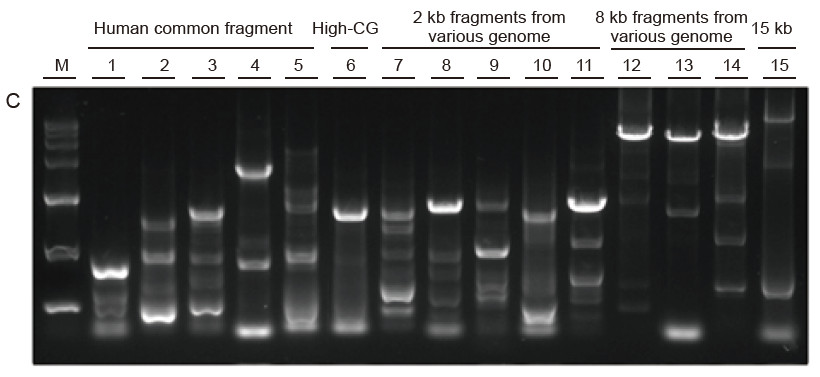 |
Sterk universalitet og høy spesifisitet, lett å lese høyt GC og lange fragmenter fra forskjellige kilder Figur 4. Ultra HiFi har høy spesifisitet for å sikre forsterkningssuksessrate og produktmengde for forskjellige typer maler. A. Ultra HiFi -forsterkningsresultater B. Hi-Fi-enzymforsterkningsresultater fra leverandør K C. Hi-Fi-enzymforsterkningsresultater fra leverandør N M: TIANGEN D15000 markør Bane 1-5. Forsterkningsresultater av maler med ulik lengde: 1. 750 bp; 2. 1 kb; 3. 2 kb; 4. 4 kb; 5. 6 kb Bane 6. Forsterkningsresultat av høy GC -mal: 1915 bp (GC%: 70%); Bane 7-11. Forsterkningsresultat av 2 kb maler fra forskjellige genom: 7. Rotte; 8. Ris; 9. Hvete; 10. Mais; 11. Bakterier; Bane 12-14. 8 kb langt fragment forsterkningsresultat: 12. Ris; 13. Mais; |
A-1 mal
■ Malen inneholder proteinforurensninger eller Taq -hemmere, etc. —— Rens DNA -malen, fjern proteinforurensninger eller ekstraher mal -DNA med rensingssett.
■ Denatureringen av malen er ikke fullført —— Øk denatureringstemperaturen passende og forleng denatureringstiden.
■ Nedbrytning av maler —— Klargjør malen på nytt.
A-2 Primer
■ Dårlig kvalitet på primere —— Syntetiser primeren på nytt.
■ Nedbrytning av primer —— Del væskene med høy konsentrasjon i lite volum for konservering. Unngå å fryse og tine flere ganger eller ved langvarig 4 ° C kryokonservering.
■ Ukorrekt utforming av primere (f.eks. Primerlengde ikke tilstrekkelig, dimer dannet mellom primere, etc.) -Resign primere (unngå dannelse av primer dimer og sekundær struktur)
A-3 mg2+konsentrasjon
■ Mg2+ konsentrasjonen er for lav —— Riktig økning av Mg2+ konsentrasjon: Optimaliser Mg2+ konsentrasjon ved en rekke reaksjoner fra 1 mM til 3 mM med et intervall på 0,5 mM for å bestemme den optimale Mg2+ konsentrasjon for hver mal og primer.
A-4 Utglødningstemperatur
■ Den høye glødetemperaturen påvirker bindingen av primer og mal. —— Reduser glødetemperaturen og optimaliser tilstanden med en gradient på 2 ° C.
A-5 Forlengelsestid
■ Kort forlengelsestid —— Øk forlengelsestiden.
Fenomener: Negative prøver viser også målsekvensbåndene.
A-1 Forurensning av PCR
■ Kryssforurensning av målsekvens eller forsterkningsprodukter —— Forsiktig å ikke pipette prøven som inneholder målsekvensen i den negative prøven eller søl dem ut av sentrifugerøret. Reagensene eller utstyret bør autoklaveres for å eliminere eksisterende nukleinsyrer, og forekomsten av forurensning bør bestemmes gjennom negative kontrollforsøk.
■ Reagensforurensning —— Alikvoter reagensene og oppbevar ved lav temperatur.
A-2 Primer
■ Mg2+ konsentrasjonen er for lav —— Riktig økning av Mg2+ konsentrasjon: Optimaliser Mg2+ konsentrasjon ved en rekke reaksjoner fra 1 mM til 3 mM med et intervall på 0,5 mM for å bestemme den optimale Mg2+ konsentrasjon for hver mal og primer.
■ Feil primerutforming, og målsekvensen har homologi med ikke-målsekvensen. —— Re-design primere.
Fenomener: PCR-forsterkningsbåndene er uforenlige med den forventede størrelsen, enten store eller små, eller noen ganger oppstår både spesifikke forsterkningsbånd og uspesifikke forsterkningsbånd.
A-1 Primer
■ Dårlig primerspesifisitet
—— Re-design primer.
■ Grunnkonsentrasjonen er for høy —— Øk denatureringstemperaturen riktig og forleng denatureringstiden.
A-2 mg2+ konsentrasjon
■ Mg2+ konsentrasjonen er for høy —— Reduser Mg2+ -konsentrasjonen riktig: Optimaliser Mg2+ konsentrasjon ved en rekke reaksjoner fra 1 mM til 3 mM med et intervall på 0,5 mM for å bestemme den optimale Mg2+ konsentrasjon for hver mal og primer.
A-3 termostabil polymerase
■ Overdreven enzymmengde —— Reduser enzymmengden på passende måte med intervaller på 0,5 U.
A-4 Utglødningstemperatur
■ Glødningstemperaturen er for lav —— Øk glødetemperaturen på riktig måte, eller bruk to-trinns glødemetode
A-5 PCR-sykluser
■ For mange PCR -sykluser —— Reduser antallet PCR -sykluser.
A-1 Primer——Dårlig spesifisitet ——Resign primeren, endre posisjonen og lengden på primeren for å forbedre dens spesifisitet; eller utføre nestet PCR.
A-2 Mal-DNA
——Malen er ikke ren —— Rens malen eller ekstraher DNA med rensesett.
A-3 mg2+ konsentrasjon
——Mg2+ konsentrasjonen er for høy —— Reduser Mg riktig2+ konsentrasjon: Optimaliser Mg2+ konsentrasjon ved en rekke reaksjoner fra 1 mM til 3 mM med et intervall på 0,5 mM for å bestemme den optimale Mg2+ konsentrasjon for hver mal og primer.
A-4 dNTP
—— Konsentrasjonen av dNTP er for høy —— Reduser konsentrasjonen av dNTP på riktig måte
A-5 Utglødningstemperatur
—— For lav glødetemperatur —— Øk glødetemperaturen passende
A-6 sykluser
—— For mange sykluser —— Optimaliser syklusnummeret

Det første trinnet er å velge riktig polymerase. Vanlig Taq-polymerase kan ikke korrekturleses på grunn av mangel på 3'-5 'eksonukleaseaktivitet, og mismatch vil i stor grad redusere forlengelseseffektiviteten til fragmenter. Derfor kan vanlig Taq -polymerase ikke effektivt amplifisere målfragmenter større enn 5 kb. Taq -polymerase med spesiell modifikasjon eller annen high fidelity -polymerase bør velges for å forbedre forlengelseseffektiviteten og dekke behovene til lang fragmentforsterkning. I tillegg krever forsterkningen av lange fragmenter også tilsvarende justering av primerdesign, denatureringstid, forlengelsestid, buffer-pH, etc. Vanligvis kan primere med 18-24 bp føre til bedre utbytte. For å forhindre malskade, bør denatureringstiden ved 94 ° C reduseres til 30 sekunder eller mindre per syklus, og tiden for å stige temperaturen til 94 ° C før forsterkning bør være mindre enn 1 min. Videre kan innstilling av forlengelsestemperaturen til omtrent 68 ° C og utforming av forlengelsestiden i henhold til hastigheten på 1 kb/min sikre effektiv forsterkning av lange fragmenter.
Feilraten for PCR -forsterkning kan reduseres ved å bruke forskjellige DNA -polymeraser med høy kvalitet. Blant alle Taq DNA -polymerasene som er funnet så langt, har Pfu -enzymet den laveste feilraten og den høyeste troverdigheten (se vedlagte tabell). I tillegg til enzymvalg kan forskere ytterligere redusere PCR -mutasjonshastigheten ved å optimalisere reaksjonsbetingelsene, inkludert optimalisering av buffersammensetning, konsentrasjon av termostabil polymerase og optimalisering av PCR -syklusnummer.
Produktkategorier
HVORFOR VELGE OSS
Siden etableringen har fabrikken utviklet produkter i førsteklasses klasse med prinsippet
av kvalitet først. Våre produkter har fått et godt rykte i bransjen og er verdifulle blant nye og gamle kunder.